Энтропия — одно из основных понятий термодинамики, являющееся мерой беспорядка или степени хаоса в системе. Введена в научный оборот Рудольфом Клаузиусом в середине XIX века, энтропия играет важную роль в понимании принципов термодинамики и ее приложений.
Согласно второму началу термодинамики, энтропия в изолированной системе может только возрастать или оставаться постоянной, но никогда не уменьшаться. Это означает, что в системе процессы, направленные на увеличение энтропии, преобладают над процессами, направленными на ее снижение. Таким образом, энтропия является фундаментальной характеристикой, описывающей естественность и планировку процессов в природе.
Значение энтропии в термодинамике простирается далеко за пределы науки. Увеличение энтропии связано с процессами, которые происходят во всех сферах нашей жизни. От холодильников, в которых тепло передается от более холодной зоны к более теплой, до распада органической материи, от которого получается энергия — все это основано на простом принципе роста энтропии.
Видео:Обратимые и необратимые процессы. Энтропия. Второй закон термодинамики. 10 класс.Скачать

Понятие энтропии
Понятие энтропии представляет собой сущность второго закона термодинамики, который утверждает, что энтропия в изолированной системе всегда возрастает или остается постоянной. Это означает, что процессы в природе направлены к увеличению энтропии.
Энтропия имеет статистическую интерпретацию. Она связана с вероятностью макроскопического состояния системы, основанной на распределении микроскопических состояний частиц. Чем больше возможных состояний системы, тем больше энтропия.
Значение энтропии в термодинамике заключается в том, что она позволяет описать направление и характер процессов, которые происходят в системе. При увеличении энтропии, система становится более неупорядоченной и менее организованной.
Роль энтропии в природе и технике заключается в том, что она позволяет предсказать и объяснить много различных явлений. Например, энтропия объясняет, почему невозможно полностью превратить все тепло в работу, почему процессы необратимы и почему химические реакции не протекают всегда в том направлении, которое мы хотим.
Термодинамическое свойство
Энтропия системы может быть положительной или отрицательной, в зависимости от степени упорядоченности или неупорядоченности ее частиц. Если система находится в упорядоченном состоянии, то энтропия будет низкой, так как вероятность такого состояния мала. Наоборот, если система находится в хаотическом состоянии, то энтропия будет высокой, так как вероятность такого состояния высока.
Термодинамические свойства системы могут быть описаны с помощью таблицы, в которой перечислены значения энтропии для различных состояний системы при разных значениях температуры и давления. Такая таблица называется «таблицей химических элементов» и имеет большое значение в химическом и физическом анализе.
| Температура (T) | Давление (P) | Энтропия (S) |
|---|---|---|
| 25 °C | 1 атм | 50 J/(mol·K) |
| 100 °C | 1 атм | 75 J/(mol·K) |
| 200 °C | 1 атм | 100 J/(mol·K) |
Такая таблица может быть использована для определения энтропии системы при известных значений температуры и давления, а также для предсказания изменения энтропии в ходе термодинамических процессов.
Термодинамическое свойство энтропии имеет большое значение не только в термодинамике, но и во многих других областях, таких как физическая химия, криогенная техника, машиностроение и другие. Понимание энтропии и ее влияния на системы позволяет более эффективно управлять и контролировать различные процессы и явления в природе и технике.
Статистическая интерпретация
Микросостояние — это конкретное состояние системы, которое определяется положением и движением каждой отдельной частицы системы. Макросостояние — это описание системы, включающее лишь некоторые статистические параметры, такие как температура, давление и объем.
Согласно статистической интерпретации, вероятность нахождения системы в определенном микросостоянии пропорциональна числу микросостояний, соответствующих данному макросостоянию. Таким образом, энтропия системы является мерой неопределенности или разнородности микросостояний, соответствующих данному макросостоянию.
Эта интерпретация позволяет объяснить связь между энтропией и вероятностями — система с большим числом микросостояний представляет собой более неопределенную систему, где вероятность попадания в определенное состояние ниже, чем в системе с меньшим числом микросостояний.
Статистическая интерпретация энтропии имеет важное значение в статистической физике и квантовой механике, где она используется для объяснения многих фундаментальных явлений и законов природы.
Видео:Энтропия. 10 класс.Скачать

Значение энтропии
Значение энтропии позволяет определить вероятность различных микросостояний системы. Чем больше энтропия, тем больше микросостояний можно реализовать. Высокая энтропия указывает на большую неопределенность и хаос в системе.
Изменение энтропии в системе можно описать с помощью второго начала термодинамики. Если система подвергается процессу, в котором увеличивается беспорядок или хаос, то ее энтропия возрастает. Если же упорядоченность системы увеличивается, то энтропия убывает.
| Термодинамический процесс | Изменение энтропии |
|---|---|
| Изотермический процесс | Остается постоянной |
| Адиабатический процесс | Может возрастать или убывать |
| Изохорный процесс | Убывает |
| Изобарный процесс | Может возрастать или убывать |
Знание значения энтропии позволяет предсказать, как будет происходить термодинамический процесс и как система будет вести себя в различных условиях. Энтропия играет важную роль в природе и технике, и ее понимание позволяет разрабатывать более эффективные системы и процессы.
Изменение энтропии в системе
Если в систему поступает тепло, то энтропия системы увеличивается. Это объясняется тем, что с ростом температуры частицы системы начинают двигаться быстрее и занимают больше возможных положений. В итоге возрастает количество микро состояний системы, что приводит к увеличению энтропии.
Если в системе происходит совершение работы над окружающей средой или окружающая среда совершает работу над системой, то также происходит изменение энтропии. При совершении работы энергия системы превращается в работу и ее энергетическое состояние меняется. Вместе с этим меняется и энтропия системы, так как изменяется количество микро состояний системы.
Изменение энтропии системы может быть положительным или отрицательным. Положительное изменение энтропии означает увеличение хаоса и неупорядоченности в системе. Отрицательное изменение энтропии означает уменьшение хаоса и увеличение упорядоченности.
Изменение энтропии в системе может быть связано с изменением ее температуры. По второму началу термодинамики, энтропия не может убывать в изолированной системе. Это означает, что процессы, в которых происходит уменьшение энтропии системы, невозможны без внешних воздействий.
Изменение энтропии в системе имеет важное значение в технике и природе. В технике энтропия используется для определения эффективности различных процессов, таких как теплообмен, сжатие газов и приводы. В природе энтропия определяет направление различных физических и химических процессов, включая выравнивание температур, диффузию и химические реакции.
Связь с термодинамическими процессами
Первый закон термодинамики устанавливает, что энергия в системе сохраняется, то есть она может только переходить из одной формы в другую. Энтропия в данном случае является показателем беспорядка в системе, и ее увеличение связано с неравновесными процессами и потерей полезной энергии.
Второй закон термодинамики вводит понятие энтропийного производства. Он гласит, что энтропия замкнутой изолированной системы может только увеличиваться или оставаться постоянной. Это обусловлено тем, что процессы, связанные с увеличением энтропии, являются естественными и происходят самопроизвольно, в то время как процессы, направленные на уменьшение энтропии, требуют затрат энергии.
Термодинамические процессы, такие как нагрев, охлаждение, смешение веществ, изотермическое и изохорное сжатие или расширение, связаны с изменением энтропии в системе. Например, при нагревании температура системы и энтропия повышаются, при охлаждении — понижаются. Энтропия также играет важную роль в фазовых переходах, где происходят существенные изменения в структуре и свойствах вещества.
Управление термодинамическими процессами осуществляется с использованием термодинамических циклов, таких как цикл Карно или цикл Брэятона, которые оптимизируют использование энергии и минимизируют потери в виде энтропии. Использование энтропии в проектировании систем позволяет улучшить их эффективность и надежность.
Таким образом, энтропия является неотъемлемой частью термодинамических процессов и играет важную роль в определении условий и направления этих процессов. Понимание связи между энтропией и термодинамикой позволяет разрабатывать более эффективные технологии и системы, а также предсказывать и контролировать их поведение.
Роль энтропии в природе и технике
В природе энтропия играет важную роль, поскольку она является мерой для оценки возможности направления физических процессов. Согласно второму началу термодинамики, энтропия изолированной системы может только увеличиваться или оставаться постоянной.
Например, в различных биологических системах энтропия играет роль организации и поддержания жизненных процессов, так как она определяет направление и возможность многих физиологических реакций.
В технике энтропия также играет важную роль. Во-первых, она позволяет оптимизировать процессы и повысить эффективность систем, например, воздушных компрессоров и турбин. Определение и контроль энтропии позволяют достичь наилучшей работы этих устройств.
Во-вторых, энтропия используется для анализа различных физических систем и процессов, таких как тепловые двигатели, электростанции и прочие устройства, находящие широкое применение в технике. Знание энтропии позволяет оптимизировать их работу и повысить эффективность.
Таким образом, энтропия играет важную роль в природе и технике, позволяя оптимизировать процессы и повысить эффективность систем. Понимание и контроль этого параметра необходимы для развития современных технологий и достижения новых научных открытий.
🎦 Видео
Что такое Энтропия?Скачать

Энтропия и второй закон термодинамики (видео 6) | Энергия| БиологияСкачать

Что такое второй закон термодинамики?Скачать

Энтропия в термодинамике, EntropyСкачать
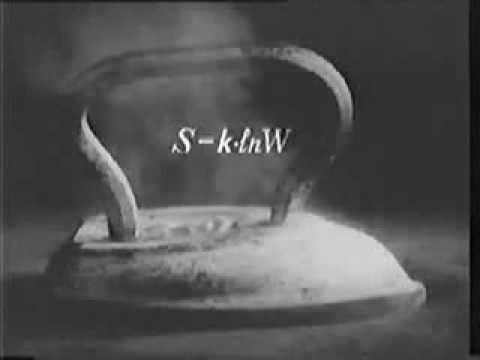
Законы Термодинамики. Что Такое Термодинамика?Скачать

Термодинамика | понятие энтропииСкачать

Второе начало термодинамики. Часть 5. Понятие энтропии.Скачать

Энтропия и вероятность. Часть 1. Макро- и микросостояния.Скачать

ФИЗИКА ЗА 5 МИНУТ - ТЕРМОДИНАМИКАСкачать

ФИЗИЧЕСКАЯ ХИМИЯ (ТЕРМОДИНАМИКА). ОСНОВНЫЕ ПОНЯТИЯ: СИСТЕМЫ, ПАРАМЕТРЫ, ФУНКЦИИСкачать

ЭнтропияСкачать

Энтропия и второе начало термодинамикиСкачать

Необратимость процессов в природе | Физика 10 класс #42 | ИнфоурокСкачать

Обратимые и необратимые процессы. Энтропия. Второй закон термодинамики. Практическая часть.10 класс.Скачать

ЭНТРОПИЯ – почему РАЗРУШАТЬ ЛЕГЧЕ, чем СОЗДАВАТЬ? // Vital MathСкачать

Энтропия на пальцах 🤏#shorts #физика | ЕГЭ 2023 по физике | Снежа ПланкСкачать

Физика. 10 класс. Обратимые и необратимые процессы. Энтропия. Второй закон термодинамики/14.12.2020/Скачать

