Испарение воды – это процесс, в ходе которого жидкость превращается в пар при достаточной температуре. Однако остается вопрос – является ли избыточная жара единственным условием или в этом процессе участвуют и химические свойства воды? Этот вопрос актуален с момента открытия испарения как феномена. Один лагерь утверждает, что испарение является исключительно физическим процессом, связанным с изменением агрегатного состояния вещества. Другие же ученые утверждают, что в процессе испарения вода расщепляется на более мелкие частицы под воздействием тепла.
Сторонники физического взгляда на испарение доказывают, что это явление объясняется исключительно изменением температуры. Поднявшись выше определенной температуры, молекулы воды получают достаточно энергии, чтобы преодолеть межмолекулярные силы и перейти в состояние газа. В этом случае изменяется только агрегатное состояние вещества, но его химические свойства остаются неизменными.
Однако противники этого взгляда предлагают совершенно иное объяснение процесса испарения. Согласно их точке зрения, испарение воды – это химическая реакция, в ходе которой молекулы воды разделяются на атомы водорода и кислорода, и только после этого преобразуются в пар при воздействии тепла. Таким образом, вода не только изменяет свое агрегатное состояние, но и проводит раздельную работу с химическими элементами, которыми она состоит.
Видео:ИспарениеСкачать

Физическое явление:
Температурная зависимость испарения воды показывает, что с увеличением температуры скорость испарения также увеличивается. Это объясняется тем, что с повышением температуры молекулы воды получают больше энергии и могут совершать более быстрые движения, что способствует их переходу в газообразное состояние.
Поверхностное явление также играет роль в процессе испарения воды. Вода обладает поверхностным натяжением, что означает, что ее молекулы на поверхности жидкости образуют пленку с сильным внутренним сцеплением. Это затрудняет выход молекул из поверхностного слоя и препятствует быстрому испарению. Однако, повышение температуры увеличивает движение молекул и помогает преодолеть поверхностное натяжение, что способствует более интенсивному испарению.
Таким образом, испарение воды является важным физическим явлением, которое происходит при определенных условиях и играет важную роль в природе и в жизни человека. С пониманием процесса испарения возможно применение этого знания в различных областях, например, в основе работы климатических систем и производственных процессов.
Процесс перехода
Процесс испарения воды имеет важное значение для земных систем, так как является ключевым фактором цикла воды. Испарение происходит с поверхности водоемов, почвы, растений и даже из поверхности тела человека. Водяной пар поднимается в атмосферу и затем конденсируется, образуя облака или возвращаясь на землю в виде осадков, таких как дождь, снег или туман. Это обеспечивает постоянный обмен воды между океанами, воздухом и сушей, обеспечивая поддержание жизни на планете.
Испарение воды также является важным процессом регулирования температуры поверхности Земли. При испарении энергия тепла поглощается водой, что приводит к охлаждению окружающей среды. Это помогает поддерживать оптимальные условия для жизни растений и животных.
Испарение воды может быть ускорено, например, ветром, поверхностным движением воды или повышенной температурой. Это может привести к образованию облаков, тумана или пыльной бури, а также к нехватке воды в регионах с низкими осадками.
Температурная зависимость испарения воды
Температура является основным фактором, влияющим на скорость испарения воды. Чем выше температура, тем быстрее происходит испарение. При этом взаимодействие молекул воды и их движение становятся более энергичными, что приводит к переходу из жидкого состояния в газообразное.
Кроме того, температура также влияет на поверхностное явление испарения воды. При повышении температуры молекулы воды получают больше энергии и активнее двигаются, что приводит к увеличению давления на поверхности воды. Это ускоряет процесс испарения.
Температурная зависимость испарения воды можно представить в виде графика. При низких температурах скорость испарения невелика, поскольку молекулы воды имеют меньше энергии. По мере повышения температуры скорость испарения увеличивается, пока не достигнет точки кипения. При этой температуре испарение происходит настолько интенсивно, что пар образуется не только на поверхности воды, но и внутри нее.
Таким образом, температурная зависимость испарения воды позволяет понять, как изменяется скорость этого процесса при изменении температуры. Это знание важно для понимания метеорологических явлений, процессов образования облаков и дождя, а также для применения в различных технологических процессах.
Поверхностное явление
Когда вода испаряется, молекулы воды преодолевают силу притяжения между ними и переходят из жидкого состояния в газообразное состояние. Однако, поверхность воды представляет собой особую зону, где молекулы воды сталкиваются с молекулами воздуха. Это приводит к образованию поверхностной пленки, которая называется поверхностным слоем.
Поверхностный слой воды имеет упругие свойства и способность к сжатию и растяжению. В нем молекулы воды ориентированы таким образом, что их заряды, связанные с положением атомов кислорода и водорода, создают притягивающие силы. Это обуславливает устойчивость поверхностного слоя и его способность удерживать другие молекулы воды.
Кроме того, поверхностное явление влияет на явления смачивания и вытекания. Например, капли воды на листьях растений образуют шарообразную форму из-за поверхностного натяжения. Это позволяет каплям дольше оставаться на поверхности и увеличивает шансы впитывания влаги растением. Также поверхностное явление обуславливает возможность использования воды в каплевидных аппаратах, таких как инжекторы или пипетки.
Таким образом, поверхностное явление играет важную роль в физико-химических свойствах воды и влияет на многие ее процессы. Изучение и понимание этого явления помогает лучше понять физику и химию воды и применить эти знания в различных областях, таких как наука, технология, медицина и окружающая среда.
Видео:Кипение и конденсацияСкачать

Химическое явление:
Химическое явление может представлять собой разложение вещества на элементы. Например, при нагревании серы она разлагается на атомы серы. Этот процесс можно описать химическим уравнением:
| S8 | → | 8S |
Таким образом, сера переходит из молекулярной формы в атомную форму.
Химическое явление также может происходить при взаимодействии веществ с другими веществами. Например, при смешении натрия и хлора образуется хлорид натрия:
| 2Na | + | Cl2 | → | 2NaCl |
При этом натрий и хлор образуют новое соединение — хлорид натрия.
Химические явления могут происходить как при повышении, так и при снижении температуры. Температура может влиять на скорость протекания химических реакций и образование определенных продуктов.
Разложение воды на элементы
Воду можно разложить на элементы с помощью специального устройства, называемого электролизером. Электролизер состоит из двух электродов — катода и анода, между которыми находится вода. При подаче электрического тока на электроды происходит разложение воды на кислород и водород.
На аноде происходит окисление воды. Кислородные ионы (O2-) при переходе на анод отделяются от своего электрода и образуют молекулы кислорода (O2). Это происходит в соответствии с реакцией:
O2- → O2 + 4e-
На катоде происходит восстановление воды. Водородные ионы (H+) при переходе на катод получают электроны и превращаются в атомы водорода (H2). Это происходит в соответствии с реакцией:
2H+ + 2e- → H2
Таким образом, разложение воды на элементы представляет собой электрохимическую реакцию, которая позволяет получить кислород и водород в свободной форме. Эти элементы могут быть использованы в различных химических и технических процессах, например, для производства водорода как энергоносителя или для получения кислорода в медицинских целях.
Взаимодействие испарения воды с другими веществами
Реакция с кислотами: Когда вода взаимодействует с кислотами, она может образовывать с ними соответствующие соли и высвобождать газы. Например, если к воде добавить серную кислоту (H2SO4), возникает реакция, в результате которой образуется сульфат магния (MgSO4) и освобождается диоксид серы (SO2) и вода:
H2O + H2SO4 → MgSO4 + SO2 + H2O
Растворение веществ: Вода обладает высокой растворяющей способностью и может взаимодействовать с различными соединениями, расщепляя их на ионы. Это важно для поддержания химического равновесия в природе. Многие минералы, соли и другие вещества могут растворяться в воде и образовывать гидратированные ионы. Например, обычная кухонная соль (NaCl) растворяется в воде, образуя натриевые и хлоридные ионы:
NaCl + H2O → Na+ + Cl-
Реакция с основаниями: Вода может реагировать с основаниями, образуя соответствующие соли и воду. Например, реакция между NaOH (гидроксид натрия) и HCl (соляная кислота) приводит к образованию натриевого хлорида (NaCl) и воды:
H2O + NaOH + HCl → NaCl + H2O
Взаимодействие испарения воды с другими веществами играет важную роль в многих химических и биологических процессах. Оно позволяет проводить различные химические реакции, растворять и переносить различные вещества в природе, а также способствует поддержанию общей водной среды в жизни на Земле.
Образование новых соединений
Испарение воды может привести к образованию новых соединений, особенно при наличии других веществ. Вода способна взаимодействовать с различными химическими соединениями, что приводит к образованию новых веществ.
Примером является реакция воды с металлами. Например, при контакте с натрием (Na), вода может прореагировать, образуя гидроксид натрия (NaOH) и выделяя водород (H2):
- 2Na + 2H2O → 2NaOH + H2
Эта реакция позволяет получать гидроксид натрия, который широко используется в различных отраслях промышленности.
Вода также может образовывать новые соединения при взаимодействии с газами, например, при смешении воды и углекислого газа (CO2) образуется угольная кислота (H2CO3):
- CO2 + H2O ⇌ H2CO3
Угольная кислота играет важную роль в биологических процессах и может быть использована в различных химических реакциях.
Кроме того, вода может образовывать соединения при взаимодействии с другими веществами, например, солями. При смешении воды и хлорида натрия (NaCl) образуется раствор соли, состоящий из ионов натрия (Na+) и хлорида (Cl-).
- NaCl + H2O → Na+ + Cl-
Образование новых соединений при испарении воды позволяет регулировать pH среды и играет важную роль во многих химических и биологических процессах.
📺 Видео
Испарение воды (физическое явление или химическое явление?) Химия 5-6 класс, естествознание 5-6 клСкачать

Физика 8 класс (Урок№8 - Испарение и конденсация. Насыщенный пар. Кипение.)Скачать

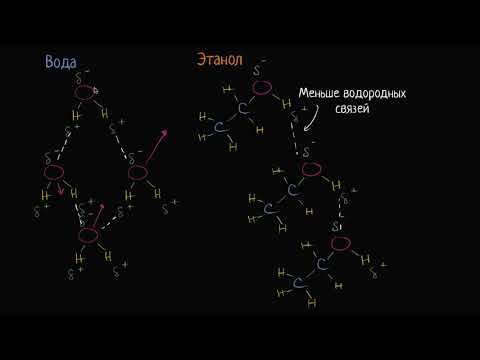
Спирт и вода. Испарение (видео 5) | Биологическая роль воды | БиологияСкачать
Физические и химические явления. 7 класс.Скачать

Химические и физические явления. | опыт | химияСкачать

Испарение. Ненасыщенный и насыщенный пар | Физика 8 класс #5 | ИнфоурокСкачать

Урок 187. Испарение и конденсация. Насыщенный пар и его свойстваСкачать

Урок 121 (осн). Испарение и конденсацияСкачать
Физика кипящего чайникаСкачать

КипениеСкачать

Урок 3. Физические и химические явления. Признаки химической реакции.Скачать

Аномальные свойства водыСкачать

Галилео. Эксперимент. Кипение перегретой водыСкачать

Три состояния вещества: жидкое, твердое, газообразное. Испарение водыСкачать

Испарение Поглощение энергии при испарении жидкости и выделение ее при конденсации пара | ФизикаСкачать

Парообразование и конденсация. 8 класс.Скачать

Химия 8 Физические и химические явленияСкачать

Про круговорот воды в природе. Познавательный мультикСкачать

