Алканы – это насыщенные углеводороды, состоящие только из атомов углерода и водорода. Их молекулы могут быть линейными или разветвленными. Хотя алканы обладают простой структурой и обычно ведут себя пассивно, они все же подвержены реакциям замещения. Эти реакции играют важную роль в химической индустрии и носят большое практическое значение.
Основной причиной подверженности алканов реакциям замещения является желание некоторых групп сырьевых химических веществ замещать атомы водорода в молекуле алкана на другие функциональные группы. Это можно объяснить высокой энергией связи между атомами углерода и водорода в алканах и более низкой энергией связи с другими атомами.
Механизмы реакций замещения в алканах могут быть различными и зависят от условий проведения реакции. Однако, основным общим фактором является наличие активного реагента, способного взаимодействовать с молекулой алкана и заместить один или несколько атомов водорода. Такие реагенты могут быть различными, например, галогены, кислородсодержащие соединения или карбоксильные кислоты.
- Причины подверженности алканов реакциям замещения
- Низкая реакционная активность алканов
- 4. — Замещение халогенами для увеличения реакционной активности
- Влияние физических условий на реакционную способность алканов
- Механизмы реакций замещения алканов
- Нуклеофильное замещение в реакциях алканов
- Электрофильное замещение алканов
- 🔥 Видео
Видео:Механизм реакций замещения | Химия ЕГЭ 10 класс | УмскулСкачать

Причины подверженности алканов реакциям замещения
Однако, некоторые факторы могут повышать реакционную способность алканов, делая их подверженными к реакциям замещения. Основные причины подверженности алканов реакциям замещения включают:
| 1. | Низкая реакционная активность алканов |
| 2. | Замещение халогенами для увеличения реакционной активности |
| 3. | Влияние физических условий на реакционную способность алканов |
Низкая реакционная активность алканов обусловлена наличием только одинарных связей между атомами углерода. Эта химическая связь является наиболее прочной и устойчивой, что делает алканы мало подверженными химическому разложению. Поэтому, для того чтобы возможно было замещение атомов водорода в алканах, необходимо применять различные методы, повышающие их реакционную активность.
Один из таких методов — замещение халогенами. Халогены, такие как хлор, бром и йод, обладают высокой химической активностью и могут принудительно вступать в реакцию с алканами. В результате замещения атомов водорода на атомы халогенов образуются галогеналканы, которые являются более реакционно активными соединениями.
Физические условия также оказывают влияние на реакционную способность алканов. Увеличение температуры и применение катализаторов способствуют повышению скорости реакции замещения атомов водорода.
В итоге, подверженность алканов к реакциям замещения обусловлена их химической структурой, однако, с помощью определенных методов, таких как замещение халогенами и изменение физических условий, эту реакционную активность можно значительно повысить.
Низкая реакционная активность алканов
Причина низкой реакционной активности алканов заключается в том, что одинарная связь между углеродами является наиболее стабильной и наименее электронно-положительной из всех типов связей в органических соединениях. В связи с этим, энергия активации для разрыва связи между углеродами в алканах очень высока, что затрудняет проведение реакций замещения.
Кроме того, углеводородные цепи алканов могут быть очень длинными, что также уменьшает реакционную активность. Длинные углеводородные цепи оказывают сильное стерическое влияние на реакции замещения, затрудняя доступность активного места для нападения реагента.
Таким образом, низкая реакционная активность алканов является следствием стабильной одинарной связи между углеродами и стерических эффектов длинных углеводородных цепей. Однако, с помощью определенных методов, таких как замещение халогенами, можно повысить их реакционную активность и внести изменения в структуру алканов.
| Свойство | Пояснение |
|---|---|
| Стабильная одинарная связь | Углероды в алканах соединены только одинарными связями, что делает их структуру стабильной и неактивной. |
| Высокая энергия активации | Разрыв связи между углеродами в алканах требует высокой энергии активации, что затрудняет проведение реакций замещения. |
| Стерические эффекты | Длинные углеводородные цепи препятствуют доступу реагентов к активному месту на молекуле алкана. |
4. — Замещение халогенами для увеличения реакционной активности
Однако, алканы могут быть подвержены реакции замещения, при которой один или несколько атомов водорода заменяются другими атомами или группами атомов. Одним из способов увеличить реакционную активность алканов является замещение атомов водорода на атомы галогенов, такие как хлор, бром или йод.
Это происходит благодаря различию в электроотрицательности атомов галогенов и атомов водорода. Атомы галогенов имеют высокую электроотрицательность и, следовательно, образуют электрофильные центры. В то же время, атомы водорода являются нуклеофильными центрами, так как у них низкая электроотрицательность.
Из-за различия в электроотрицательности, атомы галогенов могут атаковать атомы водорода в молекулах алканов. В результате замещения происходит образование новой химической связи между атомом галогенов и аольфой, а атом водорода удаляется. Это приводит к образованию галогеналканов.
Замещение атомов водорода атомами галогенов является одним из наиболее распространенных и изученных реакций замещения алканов. Эта реакция широко используется в химической промышленности для получения различных химических соединений, таких как хлорметан, бромпропан или йодбутан.
Влияние физических условий на реакционную способность алканов
Физические условия играют важную роль в процессе реакционной способности алканов. Они могут существенно влиять на скорость и направление реакций замещения.
Один из ключевых факторов — это температура. Высокая температура способствует увеличению энергии частиц, что ускоряет их движение и сталкиваемость. В результате, реакционная способность алканов увеличивается. Более высокая температура также может увеличивать вероятность активации слабых связей в молекуле алкана, что делает его более доступным для замещения.
Давление также может оказывать влияние на реакционную способность алканов. Это особенно относится к газовым алканам. Повышенное давление может увеличить скорость реакции замещения, поскольку большее количество молекул будет находиться вблизи друг друга, что способствует столкновениям.
Растворители также могут играть роль в реакционной способности алканов. Некоторые растворители могут облегчать проход реагентов через гидратный оболочку, в результате чего реакция может происходить быстрее. Также, растворители могут оказывать эффект на реакцию путем стабилизации промежуточных состояний, что может влиять на выбор механизма реакции замещения.
В общем, физические условия могут значительно влиять на реакционную способность алканов. Температура, давление и растворитель могут изменять скорость реакции, выбор механизма и направление реакции замещения.
Видео:ВСЕ ПРО АЛКАНЫ за 8 минут: Химические Свойства и ПолучениеСкачать

Механизмы реакций замещения алканов
В химии существует несколько механизмов реакций замещения алканов, которые имеют большое значение для понимания и изучения свойств и химической активности этого класса органических соединений. Реакции замещения алканов происходят за счет замещения одного атома или группы атомов в молекуле алкана другими атомами или группами атомов. Эти реакции могут включать как электрофильное, так и нуклеофильное замещение.
Нуклеофильное замещение
Одним из основных механизмов реакций замещения алканов является нуклеофильное замещение. В этом механизме, нуклеофил, обладающий лишней парой электронов, атакует электрофильный атом или группу атомов в молекуле алкана, выталкивая один атом и образуя новую связь. Процесс нуклеофильного замещения обычно происходит при наличии вещества-активатора, которое способствует образованию нуклеофила.
Электрофильное замещение
Другим распространенным механизмом реакций замещения алканов является электрофильное замещение. В этом механизме, электрофильный атом или группа атомов атакует алкан, привлекая к себе электронную плотность и образуя новую связь. Электрофильное замещение обычно происходит при наличии электрофильного реагента и при определенных условиях, таких как высокая температура или катализаторы.
Механизмы реакций замещения алканов позволяют предсказывать, объяснять и контролировать эти реакции, что имеет большое практическое значение в синтезе органических соединений и фармацевтической промышленности. Понимание механизмов реакций замещения алканов помогает улучшить эффективность реакций, выбрать оптимальные условия и уменьшить количество побочных продуктов.
Нуклеофильное замещение в реакциях алканов
В химии органических соединений алканы, как самые простые углеводороды, обладают низкой реакционной активностью. Однако, существуют механизмы, которые позволяют осуществлять замещение атомов водорода в молекуле алкана.
Одним из таких механизмов является нуклеофильное замещение. Нуклеофиль — это химическое вещество, обладающее лишь одной или несколькими свободными электронными парами, которое реагирует с электрофильной атомной или группой другого вещества. В реакциях нуклеофильного замещения, нуклеофиль атакует электрофиль, замещая его в молекуле алкана.
Чтобы произошло нуклеофильное замещение, необходима наличие следующих условий:
| 1. | Наличие электрофильной группы в молекуле алкана (например, галоген) |
| 2. | Наличие нуклеофила, способного поделиться своей электронной парой |
| 3. | Условия, обеспечивающие столкновение нуклеофила и электрофила, такие как температура и концентрация реагирующих веществ |
Механизм нуклеофильного замещения может быть разным в зависимости от реагирующих веществ и условий реакции. Однако, общим для всех механизмов является атака нуклеофила на электрофиль, образование промежуточного состояния и обмен атомов или групп веществ.
Например, в случае нуклеофильного замещения галогена в молекуле алкана, происходит атака нуклеофила на галоген, образуя промежуточное состояние. Затем, происходит обмен атомов, галоген замещается нуклеофилом, и образуется новое органическое соединение.
Нуклеофильное замещение является важным понятием в химии органических реакций, так как позволяет осуществлять замещение атомов водорода в молекуле алкана, что дает возможность изменять и модифицировать свойства и состав органических соединений.
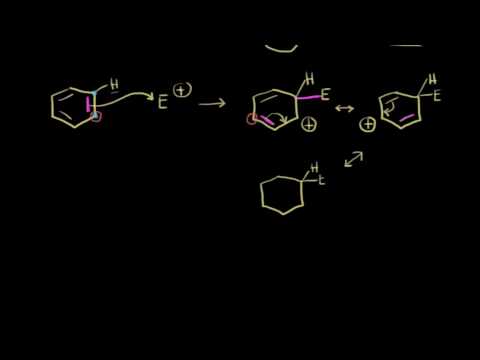
Электрофильное замещение алканов
Механизм электрофильного замещения алканов может быть разделен на несколько этапов:
- Активация электрофила — это этап, на котором электрофильный ион или молекула приобретают положительный заряд и становятся готовыми к атаке алкана.
- Атака электрофила на алкан — это этап, на котором электрофильный ион или молекула вступает в реакцию с алканом, замещая один или несколько водородных атомов.
- Получение продукта — это этап, на котором образуется новое соединение после атаки электрофила на алкан.
Примером электрофильного замещения алканов является реакция замещения метана хлором:
| Реагенты | Продукты |
|---|---|
| Метан | Хлорметан |
На первом этапе электрофильное хлоровое ион образует электрофильный центр, приобретая положительный заряд. На втором этапе хлоровый ион атакует метан, замещая один из его водородных атомов. На третьем этапе образуется новое соединение — хлорметан.
Электрофильное замещение алканов является важным процессом, используемым в органической химии для синтеза различных соединений. Эта реакция может происходить с множеством электрофилных реагентов и приводить к образованию разнообразных продуктов.
🔥 Видео
Механизм реакции РАДИКАЛЬНОГО ЗАМЕЩЕНИЯ у АЛКАНОВСкачать

Механизм Sr (радикальное замещение)Скачать

Алканы. Химические свойства. Ч.1. Реакции радикального замещения.Скачать

Галогенирование алкановСкачать

Химические свойства алканов | Химия ЕГЭ для 10 класса | УмскулСкачать

Механизм радикального замещенияСкачать

7 ВАЖНЕЙШИХ РЕАКЦИЙ, которые тебе нужно знать (Алкины)Скачать

Как решать ОРГАНИЧЕСКИЕ ЦЕПОЧКИ? Основные типы химических реакцийСкачать

СЕКРЕТЫ АЛКАНОВ РАСКРЫТЫ — Гомологи, Типы Связей, ИзомерияСкачать

Химические свойства алканов. 1 часть. 10 класс.Скачать

1.3. Алканы: Химические свойства. Подготовка к ЕГЭ по химииСкачать

Механизм электрофильного ароматического замещенияСкачать
Получение алканов. Реакция Вюрца (механизм + сложные случаи). ЕГЭ по химии.Скачать

Химические свойства алканов. Реакция окисления алканов (механизм + сложные случаи). ЕГЭ по химии.Скачать
#9. Физические и химические свойства алканов. Реакции замещенияСкачать

Механизм электрофильного замещения в ароматическом рядуСкачать

Классификация реакций: нуклеофилы, электрофилы, радикалыСкачать

Реакция ВюрцаСкачать