В химии вещества можно разделить на две большие группы: простые и сложные вещества. Простые вещества представляют собой вещества, состоящие из одного вида атомов и не могут быть разложены на более простые составляющие. Сложные вещества, наоборот, состоят из двух или более видов атомов и могут разлагаться на составные части.
Одним из основных способов различить простые и сложные вещества является анализ их химического состава. Простые вещества, как уже было отмечено, состоят из одного вида атомов. Например, кислород (O), углерод (C), водород (H) — все они являются простыми веществами. Сложные вещества, в свою очередь, имеют состав, включающий различные атомы, такие как вода (H2O) или углекислый газ (СО2).
- Основные различия между простыми и сложными веществами
- Простые вещества
- Определение и свойства простых веществ
- Примеры простых веществ:
- Сложные вещества
- Сложные вещества — определение и свойства
- Примеси в сложных веществах
- Как отличить простые и сложные вещества
- Физические свойства для отличия простых и сложных веществ
- 🎬 Видео
Видео:Химия 8 класс (Урок№4 - Атомы, молекулы и ионы. Простые и сложные вещества.Химические элементы.)Скачать

Основные различия между простыми и сложными веществами
Простые вещества состоят из одного вида атомов, которые не могут быть разделены на более простые составляющие части. Они представлены элементами периодической системы, такими как кислород, углерод, железо и другие. Каждый элемент имеет свою уникальную химическую формулу и свойства, что позволяет его идентифицировать.
Сложные вещества состоят из двух или более простых веществ, называемых компонентами. Компоненты могут быть простыми веществами или соединениями. В отличие от простых веществ, сложные вещества могут быть разделены на составляющие их компоненты путем химических реакций или физических методов.
Основные различия между простыми и сложными веществами заключаются в их составе и возможности разделения. Простые вещества имеют постоянный химический состав и не могут быть разложены на более простые части, в то время как сложные вещества имеют переменный состав и могут быть разделены на компоненты.
Простые вещества обладают химической стабильностью и определенными физическими свойствами, такими как точка плавления и кипения. Они обычно имеют определенный цвет, запах и другие характеристики, которые отличают их от других элементов. Сложные вещества могут иметь различные состояния и свойства в зависимости от их компонентов и условий окружающей среды.
Важно понимать различия между простыми и сложными веществами, так как это помогает ученым и химикам в их исследованиях, разработке новых материалов и технологий, а также понимании основных принципов химии.
Видео:Атомы и молекулы. Простые и сложные вещества. 7 класс.Скачать

Простые вещества
Простые вещества обладают уникальными химическими и физическими свойствами. Каждый элемент имеет свой уникальный атомный номер, который определяет его положение в периодической системе. Также у них может быть различная атомная масса и электронная конфигурация.
Простые вещества имеют различные формы: газы, жидкости или твердые вещества. Например, кислород — газ, железо — твердое вещество, а ртуть — жидкость.
Простые вещества могут образовывать соединения с другими элементами, образуя сложные вещества. Примерами простых веществ могут быть кислород (O), водород (H) и углерод (C).
Определение и свойства простых веществ
Простые вещества обладают рядом уникальных свойств, которые отличают их от сложных веществ.
Во-первых, простые вещества имеют постоянный химический состав. Это означает, что в простом веществе атомы одного химического элемента соединены друг с другом только этим элементом и ничем другим.
Во-вторых, простые вещества имеют определенные физические свойства, такие как точка плавления, точка кипения, плотность и т. д. Эти свойства зависят от вида простого вещества и от его молекулярной структуры.
Также простые вещества могут образовывать различные аллотропные модификации. Аллотропия — это явление, при котором простые вещества могут существовать в разных физических формах с различными структурами и свойствами. Примером аллотропии является графит и алмаз — две разные формы углерода.
Примеры простых веществ:
Кислород (O)
Кислород (O) — одно из наиболее известных простых веществ. Он является сильно реакционным газообразным элементом и составляет около 21% атмосферы Земли. Кислород относится к группе химических элементов, называемых неметаллами. Он обладает высокой электроотрицательностью и широко используется в процессе дыхания живых организмов, а также в промышленности и медицине.
Алмаз (C)
Алмаз (C) — это другой пример простого вещества. Алмаз — это природный кристаллический форма углерода, одного из самых известных химических элементов. Алмазы обладают высокой твердостью и используются в ювелирной и индустриальной областях. Они являются редкими и ценными, что делает их желанными объектами потребления.
Водород (H)
Водород (H) также является простым веществом. Он является наиболее распространенным химическим элементом во Вселенной и составляет около 75% ее массы. Водород — это легкий, цветлый и высокореакционный газ, который сгорает в контакте с кислородом, образуя воду. Водород широко используется в промышленности и является потенциальной альтернативной энергией в производстве электричества.
Это всего лишь несколько примеров простых веществ. В мире существует множество других простых веществ, каждое со своими уникальными свойствами и применениями. Изучение простых веществ играет важную роль в развитии науки и промышленности.
Видео:Простые и сложные веществаСкачать

Сложные вещества
Определение сложных веществ подразумевает наличие двух и более элементов в их составе. Эти элементы и соединения могут объединяться различными способами, образуя сложные структуры с уникальными свойствами и характеристиками.
Сложные вещества могут обладать разной степенью сложности и разнообразием составляющих их элементов. Они могут быть органическими (содержащими углерод) или неорганическими. В зависимости от состава и свойств, сложные вещества могут быть как жидкими, так и твердыми, а также могут образовывать газы при определенных условиях.
Свойства сложных веществ могут быть более сложными и разнообразными, чем у простых веществ. Они могут отличаться по таким характеристикам, как плотность, температура плавления и кипения, растворимость и электропроводность.
Примеси также могут присутствовать в сложных веществах и оказывать влияние на их свойства и характеристики. Наличие примесей может менять физические и химические свойства сложных веществ, делая их более или менее стабильными, реактивными или растворимыми.
Изучение сложных веществ имеет большое значение в химии и науке в целом, так как они являются основой для понимания химических процессов, реакций и взаимодействий, которые происходят в природе и промышленности.
Сложные вещества — определение и свойства
Сложные вещества представляют собой соединения, состоящие из двух или более элементов. Они образуются путем соединения простых веществ и имеют более сложную структуру и химический состав.
Основными свойствами сложных веществ являются:
| Свойство | Определение |
|---|---|
| Химическая реактивность | Сложные вещества могут участвовать в химических реакциях, образуя новые соединения и претерпевая изменения в своей структуре и свойствах. |
| Температурная стабильность | Сложные вещества обычно имеют более высокую температурную стабильность, чем простые вещества, и могут выдерживать более высокие температуры без распада или изменения своей структуры. |
| Физические свойства | Сложные вещества могут обладать различными физическими свойствами, такими как плотность, твердость, плавление, кипение и электропроводность. |
| Структура | Сложные вещества обычно имеют более сложную структуру, состоящую из атомов разных элементов, которые могут быть соединены различными химическими связями. |
Примерами сложных веществ являются вода (H2O), соль (NaCl), сера (S8), углекислый газ (CO2) и многие другие соединения, которые играют важную роль в химии и обладают разнообразными свойствами и применениями.
Примеси в сложных веществах
Сложные вещества могут содержать различные примеси, которые являются нежелательными или неразложимыми компонентами. Примеси могут быть представлены другими химическими элементами, соединениями или простыми веществами. Они могут находиться в сложных веществах в виде мелкодисперсных частиц, растворенных веществ или включений.
Примеси в сложных веществах могут влиять на их свойства, физическое состояние, структуру и поведение. Они могут вызывать изменение цвета, запаха, вязкости, плотности и т.д. Примеси могут также влиять на химическую активность сложных веществ и их реакционную способность.
Чаще всего примеси являются нежелательными веществами, поскольку они могут снижать качество сложных веществ и их полезные свойства. Например, примеси в металлах могут снижать их прочность, эластичность и теплопроводность. Примеси в пищевых продуктах могут вызывать аллергические реакции или снижать их пищевую ценность.
Для обнаружения и определения примесей в сложных веществах используются различные аналитические методы, такие как хроматография, спектроскопия, масс-спектрометрия и т.д. Эти методы позволяют выявить наличие и концентрацию примесей, а также провести их количественный анализ.
Избавление от примесей в сложных веществах может быть достигнуто путем проведения различных процессов очистки и переработки. Это может включать фильтрацию, дистилляцию, экстракцию и другие методы, направленные на отделение и удаление примесей.
Таким образом, примеси в сложных веществах играют важную роль в химии и технологии, поскольку они могут влиять на свойства и качество вещества. Их обнаружение и удаление являются важными задачами в химической и промышленной сферах.
Видео:Химия 8 Простые и сложные вещества Состав веществСкачать
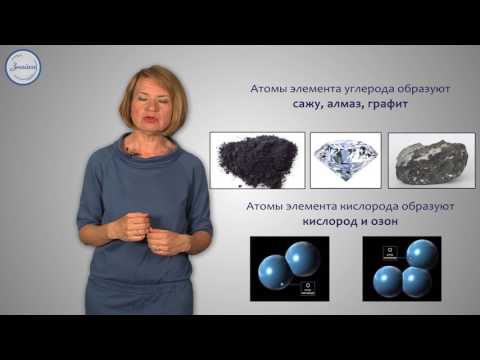
Как отличить простые и сложные вещества
Простые и сложные вещества имеют различные химические и физические свойства, которые можно использовать для их отличия.
Одним из основных методов отличия простых и сложных веществ является анализ их состава. Простые вещества состоят из одного вида атомов или молекул, тогда как сложные вещества содержат различные элементы или соединения.
Следующий метод — изменение температуры плавления или кипения. Простые вещества имеют фиксированную температуру плавления или кипения, так как их структура однородна. Сложные вещества имеют более широкие диапазоны плавления или кипения, так как их состав разнообразен.
Разности в электрических свойствах также могут помочь отличить простые и сложные вещества. Некоторые простые вещества могут быть проводниками электричества, в то время как сложные вещества обычно являются изоляторами.
Кроме того, химические реакции и возможность образования новых веществ могут быть признаками различия между простыми и сложными веществами. Простые вещества обычно не реагируют с другими веществами, в то время как сложные вещества могут образовывать новые соединения при взаимодействии с другими веществами.
В целом, отличить простые и сложные вещества можно, основываясь на их составе, температуре плавления или кипения, электрических свойствах и возможности химических реакций. Обратите внимание на эти признаки и проведите соответствующие эксперименты, чтобы определить, является ли вещество простым или сложным.
Физические свойства для отличия простых и сложных веществ
Простые вещества обычно имеют более низкую точку плавления и кипения по сравнению с соединениями. К примеру, кристаллическая фаза кислорода начинается при температуре около -218,8 °C, в то время как водородоподобный кислород имеет температуру плавления близкую к абсолютному нулю.
Простые вещества обычно не образуют никаких структурных соединений и не могут разбиться на более простые компоненты путем обычных физических процессов. Они имеют четко определенный химический состав, что также помогает в их отличии. Например, кислород всегда будет иметь формулу O2.
С другой стороны, сложные вещества, такие как углеводороды или протеины, имеют более высокие точки плавления и кипения. Они также могут иметь сложную структуру, состоящую из множества атомов разных элементов, и поэтому могут быть разложены на более простые компоненты при определенных условиях.
Определение физических свойств, таких как точка плавления, кипения, плотность или электропроводность, может помочь исследователям отличить простые вещества от сложных соединений. Эти свойства могут быть измерены с использованием различных методов и приборов, таких как термометры, весы или электрические проводники.
Таким образом, физические свойства являются важным инструментом для идентификации и отличия простых и сложных веществ. Они позволяют определить уникальные характеристики каждого вещества и помогают ученым лучше понять их структуру и свойства.
🎬 Видео
#2.Правило определения взаимодействия веществ друг с другом.Правило Бертолле. Реакции ионного обменаСкачать

7 класс. Простые и сложные вещества. Формулы: индексы и коэффициентыСкачать

1 ЗАДАНИЕ: Химический элемент и Простое вещество | Как решать БЕЗ ОШИБОК? | Химия ОГЭСкачать

ОКСИДЫ, КИСЛОТЫ, СОЛИ И ОСНОВАНИЯ ХИМИЯ 8 класс / Подготовка к ЕГЭ по Химии - INTENSIVСкачать

Простое вещество и химический элемент. В чем разницаСкачать

14. Строение веществ (простых и сложных)Скачать

Естествознание 5 Химические элементы Простые и сложные веществаСкачать

Атомы, молекулы и ионы. Простые и сложные вещества. Химические элементы. Знаки химических элементовСкачать

Типы Химических Связей — Как определять Вид Химической Связи? Химия 9 классСкачать

Урок 7. Простые и сложные вещества (8 класс)Скачать

Химия 8 класс. Простые и сложные вещества. Химический элементСкачать

Химические элементы. Простые и сложные вещества.Скачать

Вещества молекулярного и немолекулярного строения 😱 | химияСкачать

Простые и сложные веществаСкачать

§ 9. Простые и сложные вещества.Скачать

Типы Химических Реакций — Химия // Урок Химии 8 КлассСкачать

